
石家莊鑫富達醫藥包裝有限公司是專業生產塑料包裝的知名企業,公司從業二十余年,以精湛的技術、完善的管理體系、精益求精的產品服務于廣大客戶。產品遠銷到亞洲、歐洲、南北美洲等地區。是中國獸藥協會理事單位,受農業部(農業農村部)委托參與制定獸藥包裝團體標準。富于厚德,達于至善。
查看詳情1107 非無菌獸藥微生物限度標準
獸藥的微生物污染可能會導致其療效降低,甚至完全失去治療活性,并對動物健康產生不利影響。 因此,在獸藥生產、儲存和銷售過程中,需嚴格執行現行獸藥生產質量管理規范,以保證獸藥在全生命 周期中生物負載處于較低的水平。
非無菌獸藥的微生物限度標準是基于獸藥的給藥途徑和對動物健康潛在的危害以及獸藥的特殊性而 制訂的。獸藥生產、貯存、銷售過程中的檢驗,藥用原料、輔料的檢驗,新獸藥標準制訂,進口獸藥標 準復核,考察獸藥質量及仲裁等,除另有規定外,其微生物限度均以本標準為依據。
1.制劑通則、品種項下要求無菌的制劑及標示無菌的制劑和原輔料 應符合無菌檢查法規定。
2.用于手術、嚴重燒傷、嚴重創傷的局部給藥制劑 應符合無菌檢查法規定。
31.非無菌獸藥制劑的微生 物限度標準見表1。
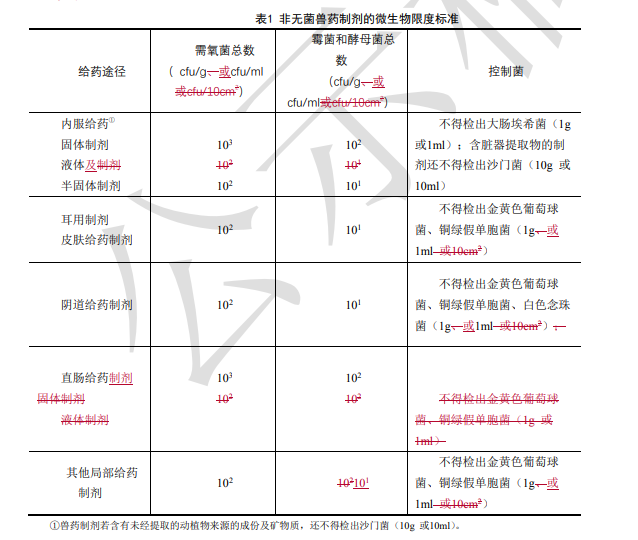
53.有兼用途徑的制劑 應符合各給藥途徑的標準。

4. 非無菌獸藥的需氧菌總數、霉菌和酵母菌總數照“非無菌產品微生物限度檢查:微生物計數法 (附錄1105)”檢查;非無菌獸藥的控制菌照“非無菌產品微生物限度檢查:控制菌檢查法(附錄 1106)”檢查。各品種項下規定的需氧菌總數、霉菌和酵母菌總數標準解釋如下:
101cfu:可接受的最大菌數為20;
102cfu:可接受的最大菌數為200;
103cfu:可接受的最大菌數為2000;依此類推。
5.本限度標準所列的控制菌對于控制某些獸藥的微生物質量可能并不全面,因此,對于原料、輔 料及某些特定的制劑,根據原輔料及其制劑的特性和用途、制劑的生產工藝等因素,可能還需檢查其他 具有潛在危害的微生物。
6.除了本限度標準所列的控制菌外,獸藥中若檢出其他可能具有潛在危害性的微生物,應從以下 方面進行評估:
獸藥的給藥途徑:給藥途徑不同,其危害不同;
獸藥的特性:獸藥是否促進微生物生長,或者獸藥是否有足夠的抑制微生物生長能力;
獸藥的使用方法;等等。
當進行上述相關因素的風險評估時,評估人員必要時,應由經過微生物學和微生物數據分析等方面 的專業知識培訓的人員進行上述相關因素的風險評估。
7. 評估原輔料微生物質量時,應考慮原輔料和相應制劑的生產工藝、現有的檢測技術、進行控制 的必要性和滿足所需質量要求原輔料的及原輔料符合該標準的必要性可獲得性。
來源:獸藥典委員會