
石家莊鑫富達醫藥包裝有限公司是專業生產塑料包裝的知名企業,公司從業二十余年,以精湛的技術、完善的管理體系、精益求精的產品服務于廣大客戶。產品遠銷到亞洲、歐洲、南北美洲等地區。是中國獸藥協會理事單位,受農業部(農業農村部)委托參與制定獸藥包裝團體標準。富于厚德,達于至善。
查看詳情本標準參照YBB00082002-2015給出的規則起草。
本標準由石家莊鑫富達醫藥包裝有限公司提出。
本標準起草單位:石家莊鑫富達醫藥包裝有限公司、滄州益康食品藥品包裝有限公司、洛陽富道生物科技有限公司。
本標準主要起草人:王錦君、趙宏蘋、賈品、王文倩、劉長喜、楊春凱。
本標準為首次發布。
獸用液體疫苗聚丙烯瓶
1 范圍
本標準規定了獸用液體疫苗聚丙烯瓶的術語、產品分類、技術要求、特性指標、試驗方法、檢驗規則、標識、包裝、運輸和貯存。
本標準適用于直接接觸獸用液體疫苗和稀釋液的包裝。
本標準適用于以聚丙烯(PP)為主要原料,采用注吹一次成型工藝生產的,可灌裝前高溫滅菌的塑料瓶。
2 規范性引用文件
下列文件對于本文件的應用是必不可少的。凡是注日期的引用文件,僅注日期的版本適用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用于本文件。GB/T2828.1-2012 計數抽樣檢驗程序 第1部分:按接收質量限(AQL)檢索的逐批檢驗抽樣計劃YBB00082002-2015 口服液體藥用聚丙烯瓶 《中華人民共和國獸藥典》2015版《中華人民共和國藥典》2015版包裝材料紅外光譜測定法(YBB00262004-2015)GB/T 191-2008包裝儲運圖示標志YBB00242005-2015環氧乙烷殘留量測定法GB15810-2001《一次性使用無菌注射器》
3 術語和定義
獸用液體疫苗聚丙烯瓶是采用聚丙烯(PP)為主要原料,采用注吹工藝生產的獸用液體疫苗包裝瓶。
4 產品規格
5-1000ml,根據客戶使用要求采用不同規格。
5 技術要求
5.1 原料
聚丙烯(PP)。
5.2 外觀質量
外觀質量要求應符合表1的規定。
表1 外觀質量要求

5.3 特性指標
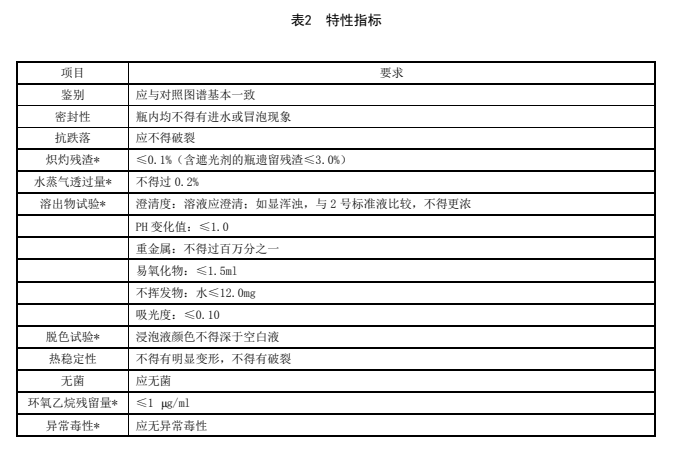
特性指標應符合表2的規定。
表2 特性指標
6 試驗方法
6.1 試驗環境
溫度0~30℃,相對濕度30~65%。
6.2 試樣抽取
在每批生產開始時取樣,按模具的腔數進行取樣,確保每腔都取到。
6.3 外觀質量
取本品適量,在自然光線明亮處,觀察者眼睛距離試樣300mm左右正視目測,觀察試樣外觀符合表1的要求。
6.4 鑒別
取本品適量,照包裝材料紅外光譜測定法(YBB00262004-2015)第四法測定,應與對照圖譜基本一致。
6.5 密封性
取本品適量,分別在瓶內裝入適量玻璃珠,加膠塞鋁蓋使用封口器封好,置于帶抽氣裝置的容器中,用水浸沒,抽真空至真空度30kpa,維持2分鐘,瓶內不得有進水或冒泡現象。
6.6 抗跌落
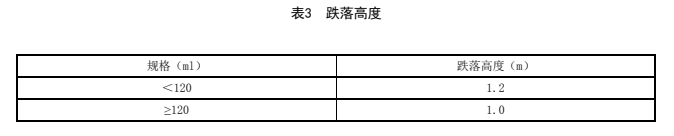
取本品適量,加入水溶液至標示容量,從規定高度(表3)自然跌落至水平剛性光滑表面,應不得破裂。
表3 跌落高度
6.7 熾灼殘渣*
取本品 2.0g,依法檢查(《中華人民共和國獸藥典》2015年版二部通則0841)遺留殘渣不得過0.1%(含遮光劑的瓶遺留殘渣不得過3.0%)。
6.8 水蒸氣透過量*
取本品適量,照水蒸氣透過量測定法(YBB00092003-2015)第三法(1)在溫度20℃±2℃,相對濕度65%±5%的條件下,放置14天,重量損失不得過0.2%。
6.9 溶出物試驗*
供試液的制備:分別取本品平整部分內表面積600cm2(分割成長 5cm ,寬 0.3cm 的小片),置具塞錐形瓶中,加水適量,振搖洗滌小片,棄去水,重復操作二次。在 30~40℃干燥后,用水(70℃±2℃)、200ml 浸泡24小時后,取出放冷至室溫,用同批試驗用溶劑補充至原體積作為供試液,以同批水為空白液,進行下列試驗 :
6.9.1 pH 變化值
取水供試液與水空白液各20ml,分別加入氯化鉀溶液(1→1000)1.0ml,依照pH 值測定法(《中華人民共和國獸藥典》2015年版二部通則0631)測定,二者差值不超過1.0。
6.9.2 重金屬
精密量取水供試液20ml,加醋酸鹽緩沖液(pH 3.5) 2ml,依法檢查(《中華人民共和國獸藥典》2015年版二部通則0821第一法),含重金屬不得過百萬分之一。
6.9.3 易氧化物
精密量取水供試液20ml,精密加入高錳酸鉀滴定液(0.002mol/L)20ml與稀硫酸1ml,煮沸3分鐘,迅速冷卻。加0.1g碘化鉀,在暗處放置5分鐘,用硫代硫酸鈉滴定液(0.01mol/L)滴定,滴定至終點時,再加入淀粉指示液5滴,繼續滴定至無色。另取水空白液同法操作,二者消耗硫代硫酸鈉滴定液(0.01mol/L)之差不得過1.5ml。
6.9.4 不揮發物
分別精密量取水供試液與空白液各50ml置于已恒重的蒸發皿中,水浴蒸干,105℃干燥2小時,冷卻后,精密稱定,水不揮發物殘渣與其空白液殘渣之差不得過12.0mg。
6.9.5 澄清度
取水供試液,依法檢查(《中華人民共和國獸藥典》2015版二部通則),溶液應澄清,如顯渾濁,與2號濁度標準液比較,不得更濃。
6.9.6 吸光度
取水供試液適量,照紫外-可見分光光度法(《中華人民共和國獸藥典》2015年版二部通則0401)測定,在220~360nm波長范圍內的最大吸光度不得過0.10。
6.10 脫色試驗(著色瓶)*
取本品適量,截取表面積50 cm2(以內表面積計)三份,剪成2cm×0.3cm的小片,分別置于3個具塞錐形瓶中,分別加入4%醋酸溶液(60℃ ±2℃)、65%乙醇(25℃±2 ℃)、正己烷(25℃±2 ℃)水浴中恒溫2小時后,取出放冷至室溫,以同批4%醋酸溶液、65% 乙醇、正己烷為空白液,浸泡液顏色不得深于空白液。
6.11 熱穩定性
(適用于灌裝前蒸汽滅菌產品)取本品適量,置高壓蒸汽滅菌器內,在15~20分鐘內由室溫均勻升至110℃,保持30分鐘或121℃,保持15分鐘。自然冷卻至高壓蒸汽滅菌器內的壓力與外界相同,打開高壓蒸汽滅菌器蓋,取出樣品觀察,不得有破裂,不得有明顯變形。
6.12 無菌
(滅菌后)取本品適量,加入1/2 標示容量的氯化鈉注射液,蓋好膠塞,振搖1分鐘,合并提取液。照無菌檢查法(《中華人民共和國獸藥典》2015年版三部附錄3306)檢查,應符合規定。
6.13 環氧乙烷殘留量*
此項目適用于采用環氧乙烷滅菌的產品。樣品制備:取本品除去包裝,吸入標示容量(V)的蒸餾水,在37℃±1℃的條件下平衡1小時。對照貯備液制備:取外部干燥的50ml容量瓶,加水30ml,加瓶塞,稱重,精確到0.1mg。用注射器注入0.6ml環氧乙烷對照品(純度大于99.7%),輕輕搖勻,再蓋好瓶塞,稱重,兩次稱重之差即為環氧乙烷重量。加水至刻度再將此溶液稀釋成1g/L作為對照貯備液。在稀釋成環氧乙烷含量為1μg/ml的溶液,作為對照液。將對照液和樣品各取5ml置頂空瓶,分別置于60℃.
6.14 異常毒性*
取本品數只,用水清洗干凈后,剪碎,取500cm2(以內表面積計),加入氯化鈉注射液50ml,置高壓蒸氣滅菌器110℃保持30分鐘后取出,冷卻后備用,以同批氯化鈉注射液做空白,靜脈注射,依法檢查(《中華人民共和國獸藥典》2015年版二部附錄1111),應符合規定。
7 檢驗規則
7.1 檢驗分類
產品檢驗分為出廠檢驗、型式檢驗、監督檢驗。
7.2 型式檢驗
7.2.1 在有下列情況之一時,應進行型式檢驗:
a) 新產品備案;
b) 產品出現重大質量事故后,重新生產;
c) 監督抽驗;
d) 產品停產后,重新恢復生產;
e) 每年至少進行一次型式檢驗;
f) 帶*項目半年內至少檢查一次。
7.2.2 型式檢驗項目應包括外觀質量、特性指標。
7.3 出廠檢驗
7.3.1 每批產品經制造商質量檢驗部門檢驗合格,并附產品合格證后方能出廠。
7.3.2 出廠檢測項目按 6.3/6.4/6.5/6.6/6.11/6.12 的要求進行產品檢驗,檢驗項目包括外觀質量、特性指標等。
7.3.3 按 GB/T 2828.1-2012 中正常檢查一次抽樣方案進行,檢驗項目、接收質量限 AQL 級檢驗水平
見表 4
7.3.4 檢驗結果中,按照計數抽樣檢驗程序第 1 部分:按接收質量限(AQL)檢索的逐批檢驗抽樣計劃(GB/T2828.1-2012)判定密封性不合格的,則判為不合格;其他項目中如有不合格的,允許加倍抽樣對不合格項目進行復檢,如復檢仍有不合格項,則判該批產品為不合格。
7.4 監督檢驗
監督檢驗時國家質量監督機構按照規定對生產廠家進行抽樣檢驗的活動。
7.5 檢驗批
用具有同一性質、質量和同一配方,并在同一連續生產周期中生產出來的一定數量的產品為一批。
8 標識、包裝、運輸、貯存
8.1 標識
每個產品的小包裝上應有下列標志:
a) 產品名稱及商標;
b) 廠名和廠址;
c) 批號、型號規格;
d) 執行標準編號;
e) 生產日期;
f) 產品大包裝上除應有以上的標志外,還應標明數量,“怕雨”﹑“怕曬”﹑“堆碼層數極限
N=8”等標志應符合 GB/T 191-2008 的有關規定。
8.2 包裝
紙箱做外包裝,塑料袋做內包裝,置干燥通風處保存。
8.3 運輸
運輸中應注意防曬,防雨雪。不得與有毒或有害物品混合運輸。
8.4 貯存
貯存環境要求應為干燥、通風良好的室內,周圍無有害或腐蝕性物品。
復驗期:24 個月。
原文下載:![]() 獸用液體疫苗聚丙烯瓶團體標準.pdf
獸用液體疫苗聚丙烯瓶團體標準.pdf